FUNÇÃO FUNDAMENTAL E GERAL DO SISTEMA [SDCTIE GRACELI] DE INTERAÇÕES, TRANSFORMAÇÕES EM CADEIAS, DECADIMENSIONAL E CATEGORIAL GRACELI.E DE ESTADOS TRANSICIONAIS =
TRANSFORMAÇÕES ⇔ INTERAÇÕES ⇔ TUNELAMENTO ⇔ EMARANHAMENTO ⇔ CONDUTIVIDADE ⇔ DIFRAÇÕES ⇔ estrutura eletrônica, spin, radioatividade, ABSORÇÕES E EMISSÕES INTERNA ⇔ Δ de temperatura e dinâmicas, transições de estados quântico Δ ENERGIAS, ⇔ Δ MASSA , ⇔ Δ CAMADAS ORBITAIS , ⇔ Δ FENÔMENOS , ⇔ Δ DINÂMICAS, ⇔ Δ VALÊNCIAS, ⇔ Δ BANDAS, Δ entropia e de entalpia, E OUTROS.
x
[EQUAÇÃO DE DIRAC].
+ FUNÇÃO TÉRMICA.
+ FUNÇÃO TÉRMICA.
+ FUNÇÃO DE RADIOATIVIDADE
, + FUNÇÃO DE TUNELAMENTO QUÂNTICO.
+ ENTROPIA REVERSÍVEL
+ FUNÇÃO DE CONDUÇÃO ELETROMAGNÉTICA
ENERGIA DE PLANCK
X
V [R] [MA] = Δe,M, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM......ΤDCG XΔe, ΔM, Δf, ΔE, Δt, Δi, ΔT, ΔC, ΔE,ΔA, ΔD, ΔM...... =
xsistema de dez dimensões de Graceli +DIMENSÕES EXTRAS DO SISTEMA DECADIMENSIONAL E CATEGORIAL GRACELI.[como, spins, posicionamento, afastamento, ESTRUTURA ELETRÔNICA, e outras já relacionadas]..- DIMENSÕES DE FASES DE ESTADOS DE TRANSIÇÕES DE GRACELI.xsistema de transições de estados, e estados de Graceli, fluxos aleatórios quântico, potencial entrópico e de entalpia. [estados de transições de fases de estados de estruturas, quântico, fenomênico, de energias, e dimensional [sistema de estados de Graceli].x
número atômico, estrutura eletrônica, níveis de energia
- TEMPO ESPECÍFICO E FENOMÊNICO DE GRACELI
- x
- X
- DT l T l E l Fl dfG lN l El tf lP l Ml tfefelTa l RlLl
Afinidade eletrônica (ou eletroafinidade), propriedade periódica, é a energia que um, e somente um átomo, em estado fundamental, no estado gasoso, libera ao "ganhar" um elétron. Essa energia liberada é representada por um , a variação de entalpia do processo. Em se tratando de processos favoráveis - onde há tendência do átomo em ganhar elétron - o processo será mais exoenergético (Reação exotérmica), ou seja, haverá maior liberação de energia (o que implica um menor que zero). Segundo Mahan, Bruce M.; et. al.:
Em outras palavras, a afinidade eletrônica, A, é a quantidade mínima de energia necessária para remover um elétron de um ânion, para gerar um átomo neutro.".[1]
Os processos favoráveis são aqueles em que o ganho de elétrons levará o átomo ao preenchimento da última camada eletrônica, ou ainda, levará o átomo a completar o octeto. A teoria do octeto proposta por Linus Pauling e amplamente conhecida em química diz que os átomos (representativos) mais estáveis são aqueles com oito elétrons na última camada, ou melhor, com a última camada completa, a exemplo os gases nobres.
Observando tais propriedades, desmente-se a ideia falsa de que os gases nobres (família 18) tem afinidade eletronica igual a zero. Tal conclusão equivocada pode vir da palavra "afinidade", sugerindo que átomos estáveis "não têm afinidade eletrônica". Na verdade, a afinidade eletrônica desses gases é menor em módulo, ou melhor, o processo é menos exotérmico para qualquer átomo gasoso com octeto completo. Observe que "afinidade eletrônica zero" representa um absurdo, uma vez que a admissão de um elétron por qualquer átomo necessariamente causa variação em sua energia.
A energia liberada é diretamente proporcional à energia potencial elétrica associada ao átomo e ao elétron admitido, e mostra-se inversamente proporcional ao raio atômico. Nas famílias da tabela periódica a afinidade eletrônica aumenta em módulo conforme diminui o número de camadas, ou seja, de baixo para cima. No período, a afinidade eletrônica aumenta, em módulo, conforme o número atômico aumenta: da esquerda para a direita. Os elementos que liberam maior energia ao ganhar um elétron são os halogênios, pois são os que estão mais próximos de atingir configuração eletrônica de um gás nobre. É digno de menção que o elemento 17 da tabela periódica, o cloro (Cl), é o elemento de maior afinidade eletrônica, liberando a maior das energias ao receber um elétron.()
X
FUNÇÃO FUNDAMENTAL E GERAL DO SISTEMA [SDCTIE GRACELI] DE INTERAÇÕES, TRANSFORMAÇÕES EM CADEIAS, DECADIMENSIONAL E CATEGORIAL GRACELI.E DE ESTADOS TRANSICIONAIS
RELATIVIDADE SDCTIE GRACELI EM >
Afinidade eletrônica em matéria condensada[editar | editar código-fonte]
Ao lidarmos com física do estado sólido e ao considerarmos técnicas de análise como a Espectroscopia de fotoelétrons excitados por raios X [2], a afinidade eletrônica é definida como a energia que seria liberada caso um elétron com energia de vácuo fosse introduzido na amostra, inicialmente neutra, ficando o mesmo por esta confinado. Sendo ENTotal a energia total do sistema com N+1 elétrons, N na amostra, neutra e em seu equilíbrio termodinâmico, e EN+1Total a energia total do sistema em seu novo equilíbrio termodinâmico após a admissão do elétron, antes estático ao nível de vácuo, e após a liberação da energia envolvida no processo de admissão, temos:
-
- χ = ENTotal − EN+1Total
- X
- FUNÇÃO FUNDAMENTAL E GERAL DO SISTEMA [SDCTIE GRACELI] DE INTERAÇÕES, TRANSFORMAÇÕES EM CADEIAS, DECADIMENSIONAL E CATEGORIAL GRACELI.E DE ESTADOS TRANSICIONAIS
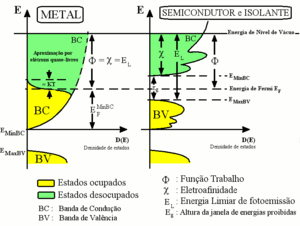
Um elétron, ao ser introduzido no sólido, deve ocupar, assumindo o equilíbrio termodinâmico, o primeiro estado disponível em energia, ou seja, o estado desocupado com menor energia na banda de condução. A eletroafinidade corresponde portanto à diferença de energias entre o nível de vácuo e a energia do primeiro estado livre, o menos energético dentro da banda de condução do sólido. No caso de metais, equipara-se à energia de Fermi. Em semicondutores, corresponde à diferença de energias entre o nível de vácuo e a energia mínima da banda de condução.
RELATIVIDADE SDCTIE GRACELI EM:
A configuração eletrônica (português brasileiro) ou configuração eletrónica (português europeu) de um átomo ou íon é uma descrição da distribuição dos seus elétrons por nível de energia.[1][2]
As configurações eletrônicas descrevem cada elétron como se movendo independentemente em um orbital, em um campo médio criado por todos os outros orbitais. Matematicamente, as configurações são descritas pelos determinantes de Slater ou pelas funções do estado de configuração.
De acordo com as leis da mecânica quântica, para sistemas com apenas um elétron, um nível de energia está associado a cada configuração eletrônica e, em certas condições, os elétrons podem passar de uma configuração para outra pela emissão ou absorção de um quantum de energia, na forma de um fóton.
O conhecimento da configuração eletrônica de diferentes átomos é útil para entender a estrutura da tabela periódica dos elementos e também para descrever as ligações químicas que mantêm os átomos unidos. Em materiais, essa mesma ideia ajuda a explicar as propriedades peculiares dos lasers e semicondutores.
Níveis de energia[editar | editar código-fonte]
A configuração eletrônica foi inicialmente concebida sob o modelo de Bohr do átomo, e ainda é comum falar de camadas e subcamadas apesar dos avanços no entendimento da natureza quântico-mecânica dos elétrons.
A coroa ou eletrosfera está dividida em 7 camadas designadas por ou pelos números: . O número de camada é chamado número quântico principal ().[2]
X
FUNÇÃO FUNDAMENTAL E GERAL DO SISTEMA [SDCTIE GRACELI] DE INTERAÇÕES, TRANSFORMAÇÕES EM CADEIAS, DECADIMENSIONAL E CATEGORIAL GRACELI.E DE ESTADOS TRANSICIONAIS
Número máximo de elétrons em cada nível de energia:
1. Teórico:
-
- O fator dois surge porque os estados permitidos são duplicados devido ao spin do elétron - cada orbital atômico admite até dois elétrons idênticos com spin oposto, um com spin +½ (geralmente denotado por uma seta para cima) e um com um spin -½ (com uma seta para baixo).
2. Experimental: O elemento de número atômico 118, chamado oganessônio, apresenta o seguinte número de elétrons nas camadas energéticas:
Camada de valência é a camada mais externa do átomo e pode contar no máximo 8 elétrons. O facto de o número máximo de elétrons no último orbital só possa ser 8, afirmação averiguada no grupo dos gases nobres da tabela periódica, leva à aplicação de uma nova camada elétrica na respetiva nuvem eletrónica, no caso do seguimento de um elemento químico correspondente a um nº atómico maior.
Subcamadas ou subníveis de energia[editar | editar código-fonte]
- X
- FUNÇÃO FUNDAMENTAL E GERAL DO SISTEMA [SDCTIE GRACELI] DE INTERAÇÕES, TRANSFORMAÇÕES EM CADEIAS, DECADIMENSIONAL E CATEGORIAL GRACELI.E DE ESTADOS TRANSICIONAIS
Nos átomos dos elementos conhecidos, os subníveis teóricos estão vazios.
Número máximo de elétrons em cada subnível experimental:
Distribuição dos elétrons nos subníveis[editar | editar código-fonte]
Os subníveis são preenchidos em ordem crescente de energia (ordem energética). Linus Pauling descobriu que a energia dos subníveis cresce na ordem:
- … [2]
É nessa ordem que os subníveis são preenchidos. Para obter essa ordem basta seguir as diagonais no Diagrama de Pauling, que afirma que não há dois elétrons no mesmo átomo que possam ter os mesmos valores dos quatro números quânticos.[3][4]
Um estado quântico é qualquer estado possível em que um sistema mecânico quântico possa se encontrar. Um estado quântico plenamente especificado pode ser descrito por um vetor de estado, por uma função de onda ou por um conjunto completo de números quânticos para um dado sistema. Vetores de estado quântico, na interpretação mais comum da mecânica quântica, não têm realidade física. O que tem significado físico são as probabilidades que podem ser calculadas a partir deles e não os vetores em si.[1] Ao estado quântico de menor energia possível dá-se o nome de estado quântico fundamental.
Na física quântica, o estado quântico se refere ao estado de um sistema isolado. Um estado quântico fornece uma distribuição de probabilidade para o valor de cada observável, ou seja, para o resultado de cada medida possível no sistema. O conhecimento do estado quântico juntamente com as regras para a evolução do sistema no tempo esgota tudo o que se pode prever sobre o comportamento do sistema.
Uma mistura de estados quânticos é novamente um estado quântico. Os estados quânticos que não podem ser escritos como uma mistura de outros estados são chamados estados quânticos puros, todos os outros estados são chamados de estados quânticos mistos.
Matematicamente, um estado quântico puro pode ser representado por um raio em um espaço de Hilbert sobre os números complexos.[2] O raio é um conjunto de vetores diferentes de zero diferindo apenas por um fator escalar complexo; qualquer um deles pode ser escolhido como um vetor de estado para representar o raio e, portanto, o estado. Um vetor unitário é normalmente escolhido, mas seu fator de fase pode ser escolhido livremente de qualquer maneira. No entanto, esses fatores são importantes quando vetores de estado são adicionados para formar uma superposição.
O espaço de Hilbert é uma generalização do espaço euclidiano comum [3] e contém todos os possíveis estados quânticos puros do sistema dado[4]. Se este espaço de Hilbert, por escolha de representação (essencialmente uma escolha de base correspondente a um conjunto completo de observáveis), é exibido como um espaço de função (um espaço de Hilbert por direito próprio), então os representantes são conhecidos como funções de onda.
Por exemplo, quando se trata do espectro de energia do elétron em um átomo de hidrogênio, os vetores de estado relevantes são identificados pelo número quântico principal n, o número quântico do momento angular l, o número quântico magnético m, e o spin z. Um caso mais complicado é dado (na notação bra-ket) pela parte de spin de um vetor de estado:
- X
- FUNÇÃO FUNDAMENTAL E GERAL DO SISTEMA [SDCTIE GRACELI] DE INTERAÇÕES, TRANSFORMAÇÕES EM CADEIAS, DECADIMENSIONAL E CATEGORIAL GRACELI.E DE ESTADOS TRANSICIONAIS
que evolve para a superposição dos estados de spin conjunto para duas partículas com spin 1⁄2.
Um estado quântico misto corresponde a uma mistura probabilística de estados puros; no entanto, diferentes distribuições de estados puros podem gerar estados mistos equivalentes (isto é, fisicamente indistinguíveis). Os estados mistos são descritos pelas chamadas matrizes de densidade. Um estado puro também pode ser reformulado como uma matriz de densidade; desta forma, os estados puros podem ser representados como um subconjunto dos estados mistos mais gerais.
Por exemplo, se o spin de um elétron é medido em qualquer direção, por exemplo com um experimento de Stern-Gerlach, há dois resultados possíveis: para cima ou para baixo. O espaço de Hilbert para o spin do elétron é, portanto, bidimensional. Um estado puro aqui é representado por um vetor complexo bidimensional , com um comprimento de um; isto é, com
- X
- FUNÇÃO FUNDAMENTAL E GERAL DO SISTEMA [SDCTIE GRACELI] DE INTERAÇÕES, TRANSFORMAÇÕES EM CADEIAS, DECADIMENSIONAL E CATEGORIAL GRACELI.E DE ESTADOS TRANSICIONAIS
onde e são valores absolutos e . Um estado misto, neste caso, tem a estrutura de uma matriz isso é, hermitiano, positivo-definido, e tem o traço 1.
Antes que uma medição particular seja realizada em um sistema quântico, a teoria geralmente fornece apenas uma distribuição de probabilidade para o resultado, e a forma que essa distribuição assume é completamente determinada pelo estado quântico e pelo observável que descreve a medição. Essas distribuições de probabilidade surgem tanto para estados mistos quanto para estados puros: é impossível na mecânica quântica (ao contrário da mecânica clássica) preparar um estado no qual todas as propriedades do sistema sejam fixas e certas. Isso é exemplificado pelo princípio da incerteza e reflete uma diferença central entre a física clássica e a física quântica. Mesmo na teoria quântica, no entanto, para todo observável existem alguns estados que têm um valor exato e determinado para aquele observável.[3][5]
Transição de Níveis de Energia[editar | editar código-fonte]
Elétrons em átomos e moléculas podem trocar (fazer transição) de níveis de energia ao emitirem ou absorverem um fóton, ou radiação eletromagnética, tal energia deve ser exatamente igual à diferença energética entre os dois níveis. Elétrons podem também ser completamente removidos de uma espécie química, como um átomo, molécula, ou íon. A remoção completa de um elétron de um átomo pode ser uma forma de ionização, que é efetivamente mover o elétron para um orbital com um número quântico principal infinito, tão longe de forma a praticamente não ter efeito algum sobre o átomo remanescente (íon). Para vários tipos de átomos, existem a 1ª, 2ª, 3ª energia de ionização e assim por diante, que podem ser fornecidas ao átomo em estado fundamental para remover elétrons do menor ao maior nível de energia. Energia em quantidades opostas também pode ser liberada, muitas vezes em forma de energia fotoelétrica, quando elétrons entram em contato com ións positivamente carregados (ou átomos). Moléculas também podem passar por transições em seus níveis de energia vibracionais e rotacionais. A transição de nível de energia também pode ser não-radioativa, significando que não ocorre a emissão ou absorção de um fóton.
Se um átomo, íon ou molécula está no menor nível de energia possível, ele e seus elétrons são ditos em estado fundamental. Se estão no maior nível de energia, são ditos excitados, ou qualquer elétron possui uma energia maior que o estado fundamental está excitado. Tal espécie pode ser excitada a um nível de energia maior ao absorver um fóton cuja energia é igual a diferença de energia entre dois níveis. Por outro lado, uma espécie pode ir para um nível de energia inferior ao emitir espontaneamente um fóton com energia igual a diferença energética. A energia de um fóton é igual a constante de Plank (h) vezes a sua frequência (f) e, portanto, é proporcional a sua frequência, ou inversamente proporcional ao seu comprimento de onda (λ).
X
FUNÇÃO FUNDAMENTAL E GERAL DO SISTEMA [SDCTIE GRACELI] DE INTERAÇÕES, TRANSFORMAÇÕES EM CADEIAS, DECADIMENSIONAL E CATEGORIAL GRACELI.E DE ESTADOS TRANSICIONAIS
 [EQUAÇÃO DE DIRAC].
[EQUAÇÃO DE DIRAC].
 + FUNÇÃO DE RADIOATIVIDADE
+ FUNÇÃO DE RADIOATIVIDADE
 + FUNÇÃO DE TUNELAMENTO QUÂNTICO.
+ FUNÇÃO DE TUNELAMENTO QUÂNTICO. + ENTROPIA REVERSÍVEL
+ ENTROPIA REVERSÍVEL ![\sigma =q(n\mu _{n}+p\mu _{p})[\Omega .cm]^{{-1}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/53d1173dd9d9ec55715f1f4beb1ea5dcd4932bc8) FUNÇÃO DE CONDUÇÃO ELETROMAGNÉTICA
FUNÇÃO DE CONDUÇÃO ELETROMAGNÉTICA ENERGIA DE PLANCK
ENERGIA DE PLANCK